Anvisa libera testes da Covaxin no Brasil e Ministério da Saúde compra 20 mil doses. Vacina da Índia ainda não tem aprovação no país
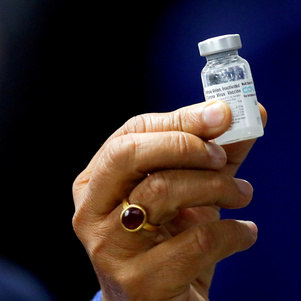
O Estado de São Paulo terá 3 mil voluntários para estudo clínico da vacina Covaxin (BBV152), contra covid-19, que foi autorizado pela Anvisa (Agência Nacional de Vigilância Sanitária) autorizou, nesta quinta-feira (13).
Segundo a Agência Nacional de Vigilância Sanitária, o estudo prevê a aplixação de duas doses do imunizante, com intervalo de 28 dias. Além dos paulistas, vão participar do estudo 500 voluntários do Rio de Janeiro, 500 da Bahia e 500 do Mato Grosso.
O estudo da vacina também está sendo conduzido na Índia com outros 26.300 mil voluntários, totalizando 30.800 voluntários no estudo global.
O pedido de autorização do estudo no Brasil havia sido feito pela Precisa Medicamentos, importadora e distribuidora de medicamentos, de São Paulo, que representa o imunizante no país.
Em nota, a Anvisa informou que o estudo é o de fase 3, que avalia a eficácia e segurança da vacina em adultos acima de 18 anos.
“Para esta autorização, a Anvisa analisou os dados das etapas anteriores de desenvolvimento dos produtos, incluindo estudos não clínicos in vitro e em animais, bem como dados preliminares de estudos clínicos em andamento. Os resultados obtidos até o momento demonstraram um perfil de segurança aceitável das vacinas candidatas”, disse a agência por meio de nota.
Sobre a Covaxin
A Covaxin tem 78% de eficácia comprovada contra o novo coronavírus, e é aplicada em duas doses, com intervalo de quatro semanas entre elas.
O infectologista Renato Kfouri, diretor da SBIm (Sociedade Brasileira de Imunizações) e membro do Comitê Técnico Assessor do PNI (Programa Nacional de Imunizações) do Ministério da Saúde, explica que a vacina é semelhante à CoronaVac, imunizante que já está em aplicação no Brasil.
“O vírus é cultivado em células Vero [linhagem de células utilizadas em culturas microbiológicas], para se multiplicar e crescer, e depois é desativado para inativar sua capacidade de infecção”, explica.
O Ministério da Saúde já comprou 20 milhões de doses da Covaxin. Mas, para que seja aplicado na população, é necessário que a Anvisa autorize o uso emergencial ou conceda o registro definitivo do imunizante.
Antes de o governo federal manifestar interesse pela vacina, a rede privada já havia anunciado a intenção de compra de 5 milhões de doses, segundo a ABCVAC (Associação Brasileira de Clínicas de Vacinas). No entanto, só após o registro definitivo é que o imunizante pode ser disponibilizado à rede privada.
ADNAN ABIDI/REUTERS
R7



